Βασική διαφορά: Η διάταξη των ατόμων σε ένα μόριο βοηθά στον προσδιορισμό της πολικότητάς του. Ένα μόριο λέγεται ότι είναι πολικό, αν έχει θετικό και αρνητικό φορτίο. Ένα μη πολικό μόριο είναι ένα μόριο με μικρότερο φορτίο.
Στη χημεία, η πολικότητα αναφέρεται στον διαχωρισμό μεταξύ των ηλεκτρικών φορτίων ενός μορίου ή της χημικής του ομάδας που έχει ένα ηλεκτρικό δίπολο ή πολλαπλό πόλο. Τα πολικά μόρια αλληλεπιδρούν μέσω ενδομοριακών δεσμών και δεσμών υδρογόνου. Η μοριακή πολικότητα εξαρτάται από τη διαφορά στην ηλεκτροαρνητικότητα μεταξύ των ατόμων ενός μορίου. Η πολικότητα, επίσης, προσδιορίζει έναν αριθμό φυσικών ιδιοτήτων όπως επιφανειακή τάση, σημεία τήξης και βρασμού και διαλυτότητα.
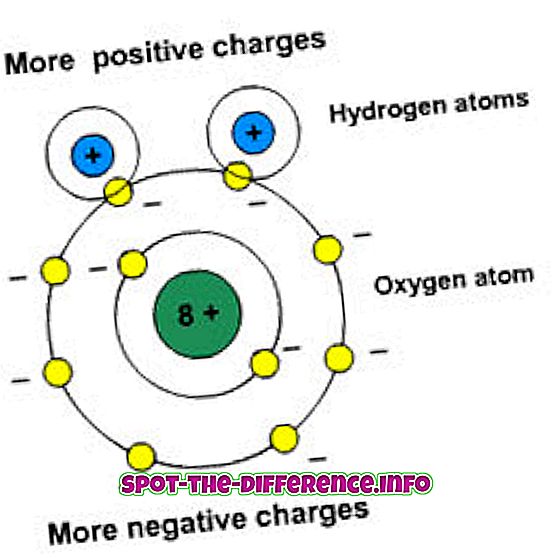
Η πολικότητα σημαίνει τον διαχωρισμό των φορτίων. Αυτά τα μόρια έχουν διπολική στιγμή. Η διπολική στιγμή μετρά την πολικότητα ενός δεσμού. Πολικές ουσίες αλληλεπιδρούν με άλλα πολικά στοιχεία.

Ένα μη πολικό μόριο δεν έχει αρκετό φορτίο. Τα μη πολικά μόρια κατανέμονται κατά τρόπο συμμετρίας και δεν έχουν μεγάλο αριθμό ηλεκτρικών φορτίων επί αυτών. Όταν δύο άτομα ή δύο ίδια άτομα έχουν τον ίδιο δεσμό ηλεκτρονίων μεταξύ τους, τα άτομα τραβούν το ζεύγος ηλεκτρονίων. Αυτή η έλξη τους βοηθά να μοιράζονται ηλεκτρόνια και αυτό το είδος κατανομής δεσμών μεταξύ των μορίων είναι γνωστό ως μη πολικοί ομοιοπολικοί δεσμοί.
Σύγκριση μεταξύ πολικών και μη πολικών:
Πολικός | Μη πολικές | |
Ορισμός | Οι πολικές ουσίες έχουν θετικό και αρνητικό φορτίο στο άτομο. | Οι μη πολικές ουσίες δεν έχουν μεγάλες ποσότητες στο συνδεδεμένο άτομο. |
Κίνηση | Έχουν ηλεκτρική κίνηση δίπολων. | Δεν έχουν καμία κίνηση δίπολων. |
Διαχωρισμός χρέωσης | Υπάρχει διαχωρισμός φορτίου. | Δεν υπάρχει διαχωρισμός χρεώσεων. |
ΑΛΛΗΛΕΠΙΔΡΑΣΗ | Συνδέονται με άλλες πολικές ουσίες. | Δεν αλληλεπιδρούν με άλλες πολικές ουσίες. |
Παράδειγμα | Νερό, αλκοόλ και θείο. | Λάδι. |