Βασική διαφορά: Τα άτομα είναι οι βασικές μονάδες από τις οποίες αποτελείται όλη η ύλη. Τα άτομα διαφορετικών στοιχείων συγκεντρώνονται για να παράγουν μόρια. Αυτό συμβαίνει μέσω μιας χημικής αντίδρασης. Ένα μόριο είναι η μικρότερη ποσότητα μιας χημικής ουσίας που μπορεί να υπάρχει. Ουσιαστικά, μια ένωση είναι ένας τύπος μορίου. Ένα μόριο μπορεί να αποτελείται από δύο ή περισσότερα άτομα του ίδιου στοιχείου ή δύο ή περισσότερα άτομα διαφορετικών στοιχείων. Ωστόσο, οι ενώσεις είναι μόρια που αποτελούνται από άτομα διαφορετικού μορίου.
Ένα στοιχείο είναι μια καθαρή χημική ουσία που έχει έναν ή έναν τύπο ατόμου, που διακρίνεται από τον ατομικό του αριθμό. Ο ατομικός αριθμός προέρχεται από τον αριθμό των πρωτονίων που υπάρχουν στον πυρήνα του στοιχείου. Υπάρχουν συνολικά 118 στοιχεία τα οποία έχουν αναγνωριστεί, τα οποία διακρίνονται μεταξύ μετάλλων, μεταλλοειδών και μη-μετάλλων. Κάθε στοιχείο έχει το δικό του σύνολο ιδιοτήτων. Τα περισσότερα στοιχεία είναι διαθέσιμα στη γη, ενώ μερικά έχουν αναπτυχθεί τεχνητά μέσω πυρηνικών αντιδράσεων. Ένα στοιχείο είναι ήδη στην πιο ακατέργαστη μορφή του και δεν μπορεί να αναλυθεί περαιτέρω. Όλα τα στοιχεία μπορούν να βρεθούν στον Περιοδικό Πίνακα, με ατομικό αριθμό.
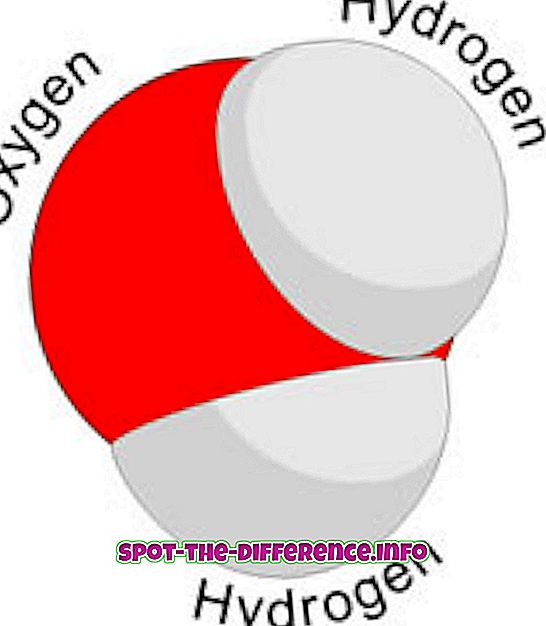
Τα άτομα διαφορετικών στοιχείων συγκεντρώνονται για να παράγουν μόρια. Αυτό συμβαίνει μέσω μιας χημικής αντίδρασης. Για παράδειγμα: δύο άτομα υδρογόνου και ένα άτομο οξυγόνου συνδυάζονται για να δημιουργήσουν ένα μόριο νερού.
Ένα μόριο είναι η μικρότερη ποσότητα μιας χημικής ουσίας που μπορεί να υπάρχει. Όπως η μικρότερη ποσότητα νερού που μπορεί κανείς να έχει είναι ένα μόριο νερού ή Η20. Είναι φτιαγμένο από διαφορετικά άτομα μαζί. Ως εκ τούτου, μπορεί να χωριστεί πίσω στα διαφορετικά άτομα.
Ένα μόριο μπορεί να έχει πολύ διαφορετικές ιδιότητες από τα στοιχεία από τα οποία αποτελείται. Για παράδειγμα: το νερό συμπεριφέρεται πολύ διαφορετικά από το οξυγόνο ή το υδρογόνο, παρόλο που αποτελείται από δύο άτομα υδρογόνου και ένα άτομο οξυγόνου.
Επιπλέον, ένα άτομο δεν μπορεί να υπάρχει ανεξάρτητα στη φύση χωρίς να δεσμεύεται σε κάτι. Ποτέ δεν θα βρούμε μόνο ένα άτομο οξυγόνου ή ένα άτομο άνθρακα. Είναι πάντα συνδεδεμένο με κάτι, όπως το O2 (οξυγόνο) ή το CO2 (διοξείδιο του άνθρακα). Όταν συνδέεται σε ένα μόριο, το μόριο μπορεί να υπάρχει ανεξάρτητα στη φύση, γι 'αυτό μπορούμε πάντα να βρούμε ένα μόριο οξυγόνου, ένα μόριο διοξειδίου του άνθρακα, ένα μόριο νερού (H2O), κλπ.

Τα μόρια τείνουν πάντα να ομαδοποιούνται, ο σχηματισμός τους εξαρτάται από την κατάσταση τους. Όπως σε αέρια κατάσταση, τα μόρια τείνουν να πετάνε απλά. Σε υγρή κατάσταση, τα μόρια τείνουν να είναι ομαδοποιημένα μεταξύ τους έτσι ώστε να μπορούν να κινηθούν. Ενώ σε στερεά κατάσταση, τα μόρια είναι γεμάτα σφιχτά μαζί και μπορούν μόνο να δονηθούν.
Τα μόρια αντιπροσωπεύονται συνήθως σε μοριακό τύπο. Για παράδειγμα: O2, H2O, CO2, C6H12O6 (ζάχαρη). Ο μοριακός τύπος είναι το όνομα του στοιχείου που ακολουθείται από τον αριθμό των ατόμων αυτού του στοιχείου στο μόριο.
Ουσιαστικά, μια ένωση είναι ένας τύπος μορίου. Ένα μόριο μπορεί να αποτελείται από δύο ή περισσότερα άτομα του ίδιου στοιχείου ή δύο ή περισσότερα άτομα διαφορετικών στοιχείων. Ωστόσο, οι ενώσεις είναι μόρια που αποτελούνται από άτομα διαφορετικών στοιχείων. Ως εκ τούτου, μπορεί να ειπωθεί ότι όλες οι ενώσεις είναι μόρια, ωστόσο δεν είναι όλα τα μόρια ενώσεις.
Επομένως, όλα τα μόρια είναι το υδρογόνο (H2), το οξυγόνο (02), το άζωτο (N2), το νερό (H2O), το διοξείδιο του άνθρακα (CO2) και το μεθάνιο (CH4). Ωστόσο, μόνο τα ύδατα (H2O), το διοξείδιο του άνθρακα (CO2) και το μεθάνιο (CH4) είναι ενώσεις, τα άλλα δεν είναι.