Βασική διαφορά: Ο ιονικός δεσμός είναι ένας χημικός δεσμός μεταξύ δύο ανόμονων (δηλ. Μεταλλικών και μη μεταλλικών) ατόμων στα οποία ένα άτομο δίνει ένα ηλεκτρόνιο στο άλλο. Ένας ομοιοπολικός δεσμός είναι ένας άλλος ισχυρός χημικός δεσμός. Γίνεται παρόμοια άτομα (δηλαδή δύο μη-μέταλλα). Σε έναν ομοιοπολικό δεσμό τα δύο άτομα έρχονται μαζί για να μοιραστούν το ηλεκτρόνιο, αντί για ένα άτομο που παίρνει ένα ηλεκτρόνιο από το άλλο.
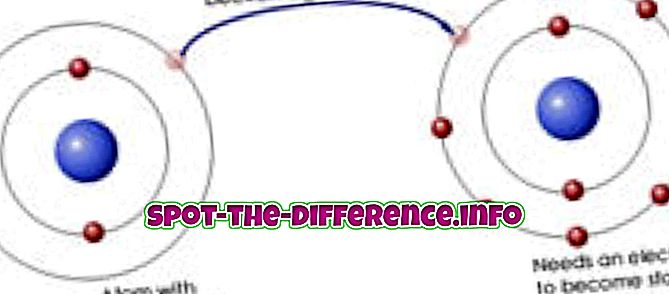
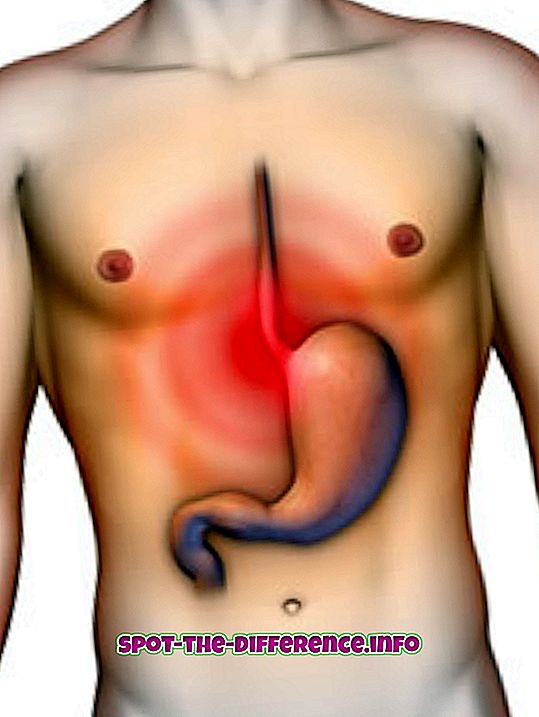
Ένας ιονικός δεσμός είναι ένας χημικός δεσμός μεταξύ δύο ανόμονων (δηλαδή μεταλλικών και μη μεταλλικών) ατόμων στα οποία ένα άτομο δίνει ένα ηλεκτρόνιο στο άλλο. Ως εκ τούτου και τα δύο άτομα γίνονται ιόντα καθώς ένα άτομο έχει ένα ηλεκτρόνιο λιγότερο, ενώ το άλλο έχει ένα επιπλέον. Το μεταλλικό ιόν που έχασε ένα ηλεκτρόνιο έχει θετικό φορτίο. Το μη μεταλλικό ιόν που απέκτησε ένα ηλεκτρόνιο έχει αρνητικό φορτίο. Καθώς τα αντίθετα προσελκύουν, αυτά τα ιόντα στη συνέχεια έλκονται έντονα μεταξύ τους, τόσο έντονα ώστε να γίνουν δεσμευμένα.
Οι ιονικές ενώσεις είναι συνήθως υπό τη μορφή στερεών, δηλαδή αλάτων. Είναι πολύ διαλυτά στο νερό και έχουν υψηλό σημείο τήξης. Όταν βρίσκονται σε νερό, έχουν επίσης υψηλή ηλεκτρική αγωγιμότητα.

Ο ομοιοπολικός δεσμός περιλαμβάνει πολλά είδη αλληλεπιδράσεων, μεταξύ των οποίων η δέσμευση σ, δέσμευση π, δέσμευση μετάλλου σε μέταλλο, αλληλεπιδράσεις με αγκίστριες και τριών κεντρικών δεσμών δύο ηλεκτρονίων. Όταν ένα άτομο έχει ένα ηλεκτρόνιο στο εξωτερικό του κέλυφος και άλλα άτομα απαιτούν ένα ηλεκτρόνιο για να γεμίσει το εξωτερικό κέλυφος του, τα δύο άτομα μαζί μαζί για να μοιραστούν το ηλεκτρόνιο. Ως εκ τούτου, και τα δύο άτομα καταλήγουν να έχουν ένα πλήρες εξωτερικό κέλυφος και αντίστοιχα μια σταθερή ηλεκτρονική διαμόρφωση.
Οι χημικοί δεσμοί γίνονται έτσι ώστε το άτομο να έχει ένα πλήρες εξωτερικό κέλυφος, καθώς ένα πλήρες εξωτερικό κέλυφος σημαίνει μια σταθερή ηλεκτρονική διαμόρφωση. Σε ένα ιοντικό δεσμό, όταν το άτομο μετάλλου έχει ένα μόνο ηλεκτρόνιο στο εξωτερικό κέλυφος του και το μη μέταλλο χρειάζεται ένα ηλεκτρόνιο για να ολοκληρώσει το εξωτερικό του κέλυφος, το άτομο μετάλλου δίνει το ηλεκτρόνιο του στο μη μέταλλο. Ομοίως, στον ομοιοπολικό δεσμό, μοιράζονται το ηλεκτρόνιο εξίσου.
Ιοντικός δεσμός | Ομοιοπολικό δεσμό | |
Ορισμός | Ένας χημικός δεσμός μεταξύ δύο διαφορετικών ατόμων στα οποία το άτομο δίνει ένα ηλεκτρόνιο στο άλλο. | Ένας ομοιοπολικός δεσμός είναι ένας χημικός δεσμός που περιλαμβάνει την κατανομή ηλεκτρονίων μεταξύ δύο παρόμοιων ατόμων. |
Περιστατικό | Ένα μέταλλο και ένα μη μέταλλο | Δύο μη-μέταλλα |
Πόλωση | Υψηλός | Χαμηλός |
Σχήμα του μορίου | Δεν υπάρχει καθορισμένο σχήμα, δομές πλέγματος | Ορισμένο σχήμα |
Ηλεκτρική αγωγιμότητα | Υψηλός | Συνήθως κανένα |
Θερμική αγωγιμότητα | Υψηλός | Συνήθως χαμηλή |
Σημείο τήξης της ουσίας | Διαφέρει, αλλά συνήθως υψηλότερο από τις ομοιοπολικές ενώσεις | Διαφέρει, αλλά συνήθως χαμηλότερο από τις ιονικές ενώσεις |
Σημείο ουσίας βρασμού | Υψηλός | Διαφέρει, αλλά συνήθως χαμηλότερο από τις ιονικές ενώσεις |
Διαλυτότητα στο νερό | Υψηλός | Διαφέρει, αλλά συνήθως χαμηλότερο από τις ιονικές ενώσεις |
Κατάσταση της ουσίας σε θερμοκρασία δωματίου | Συνήθως στερεά | Στερεό, υγρό, αέριο |