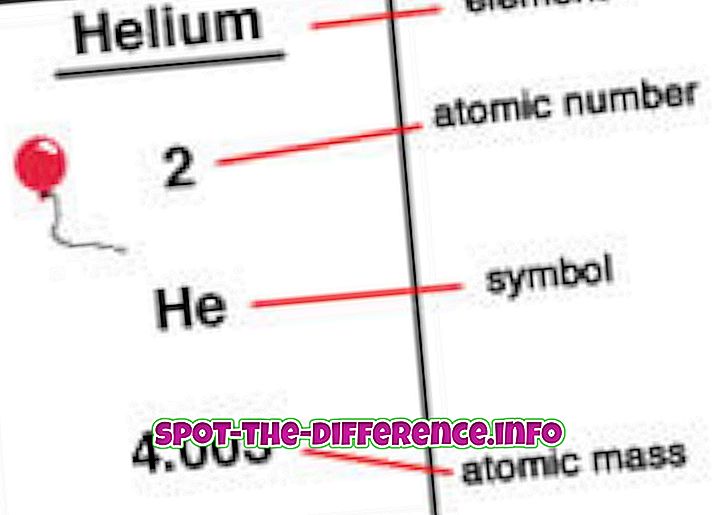
Βασική διαφορά: Η ατομική μάζα είναι απλώς η μάζα ενός συγκεκριμένου ισοτόπου ή η συνδυασμένη μάζα των πρωτονίων, των νετρονίων και των ηλεκτρονίων του ατόμου. Ο ατομικός αριθμός είναι ο αριθμός των πρωτονίων που βρίσκεται σε έναν πυρήνα ενός στοιχείου.
Ας δούμε ότι η χημεία προκαλεί σύγχυση, τα διάφορα στοιχεία, οι ατομικοί αριθμοί, οι δεσμοί, η μάζα, το βάρος, τα άτομα κλπ. Όλες αυτές οι λέξεις αρχίζουν να θολώνουν μετά από ένα ορισμένο χρονικό διάστημα που ένα άτομο δεν μπορεί πλέον να διακρίνει το ένα από το άλλο. Η ατομική μάζα και ο ατομικός αριθμός είναι δύο από αυτές τις λέξεις που συχνά συγχέονται και χρησιμοποιούνται εναλλακτικά.
Η ατομική μάζα είναι η μάζα ενός ατόμου όταν βρίσκεται σε ηρεμία. Αυτό συμβαίνει επειδή όταν ένα άτομο κινείται με πολύ μεγάλη ταχύτητα, τείνει να αυξάνεται στη μάζα. Αν και σύμφωνα με τον ορισμό, η ατομική μάζα είναι η μάζα όλων των πρωτονίων, των νετρονίων και των ηλεκτρονίων, τα ηλεκτρόνια είναι πολύ μικρά για να κάνουν οποιαδήποτε σημαντική διαφορά στην ατομική μάζα. Τα περισσότερα από τα στοιχεία του περιοδικού πίνακα έχουν ισότοπα και λόγω της διαφοράς στον αριθμό των νετρονίων, αλλάζει και η μάζα κάθε ισοτόπου.
Η ατομική μάζα εκφράζεται χρησιμοποιώντας μονάδες ατομικής μάζας ή amu. Μία μονάδα ατομικής μάζας είναι ίση με το 1 / 12ο της μάζας του άνθρακα-12. Όταν η μάζα ενός ατόμου διαιρείται με το 1 / 12ο της μάζας του Carbon-12, λαμβάνεται η σχετική μάζα του στοιχείου. Ωστόσο, η σχετική μάζα ενός αντικειμένου είναι στην πραγματικότητα το ατομικό βάρος ενός στοιχείου, όπως υπολογίζεται λαμβάνοντας υπόψη όλα τα ισότοπα. Ωστόσο, αυτό δεν πρέπει να θεωρηθεί ως ατομική μάζα ενός στοιχείου.

Ο ατομικός αριθμός είναι ο αριθμός των πρωτονίων που βρίσκεται σε έναν πυρήνα ενός στοιχείου. Όταν ένα άτομο είναι ουδέτερο, αυτό σημαίνει ότι έχει τον ίδιο αριθμό πρωτονίων και ηλεκτρονίων. Ο ατομικός αριθμός υποδηλώνεται με ένα Ζ. Δεδομένου ότι κάθε στοιχείο έχει διαφορετικό αριθμό πρωτονίων, αυτός ο αριθμός χρησιμοποιείται επίσης για να αντιπροσωπεύει ένα στοιχείο. Τα ισότοπα συνήθως μοιράζονται τον ίδιο ατομικό αριθμό αλλά ταξινομούνται χρησιμοποιώντας την ατομική τους μάζα, για παράδειγμα Carbon-12, Carbon-13.
Τα στοιχεία τοποθετούνται κατά σειρά ατομικού αριθμού σε περιοδικό πίνακα. Ο ατομικός αριθμός παρατίθεται στην επάνω αριστερή γωνία του στοιχείου ως δείκτης. Οι ατομικοί αριθμοί μπορούν να βοηθήσουν στη διάδοση πληροφοριών σχετικά με το στοιχείο και πολλοί άνθρωποι μπορούν να δουν τον ατομικό αριθμό και να δηλώσουν ποιο στοιχείο είναι. Αναφέρει επίσης πού μπορεί να τοποθετηθεί στον περιοδικό πίνακα και εάν είναι υγρό, αέριο ή στερεό. Ο ατομικός αριθμός δίνει επίσης πληροφορίες σχετικά με το φορτίο πυρήνα, τις καταστάσεις οξείδωσης, τη συμπεριφορά σύνδεσης, τη φόρτιση του ιόντος κ.λπ.