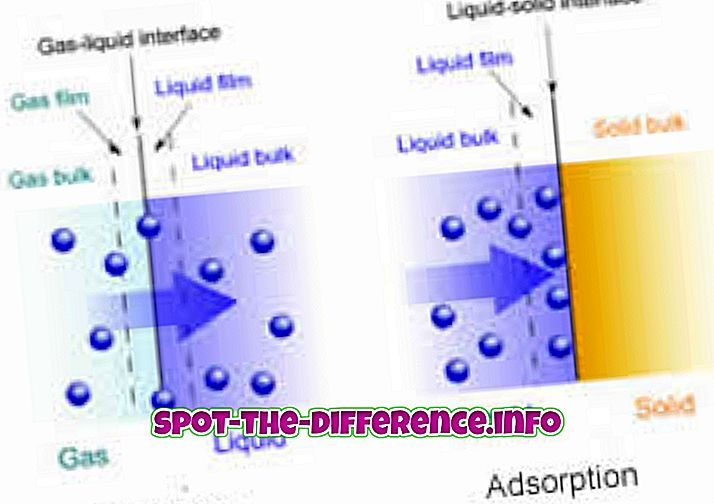
Διαφορά κλειδιού: Η απορρόφηση είναι φαινόμενο όγκου στο οποίο ένα απορροφητικό διεισδύει εντελώς στο σώμα ενός στερεού ή υγρού για να σχηματίσει μια ένωση ή ένα διάλυμα. Από την άλλη πλευρά, η προσρόφηση είναι ένα φαινόμενο επιφάνειας στο οποίο τα μόρια ενός προσροφητικού συμπυκνώνονται μόνο στην επιφάνεια ενός προσροφητικού.
Χημική Αντίδραση - διοξείδιο του άνθρακα που απορροφάται από διάλυμα ανθρακικού καλίου
Φυσική διεργασία - Ο αέρας απορροφάται στο νερό με διάλυση

Υπάρχουν δύο τύποι τρόπων απορρόφησης - χημικών και φυσικών. Στη χημική προσρόφηση τα μόρια και η επιφάνεια δεσμεύονται από τις αδύναμες δυνάμεις Vander Walls. Από την άλλη πλευρά, στη χημική προσρόφηση, σχηματίζεται ένας χημικός δεσμός μεταξύ των μορίων και της επιφάνειας.
Επομένως, η κύρια διαφορά μεταξύ προσρόφησης και απορρόφησης είναι ότι η απορρόφηση είναι φαινόμενο όγκου το οποίο σημαίνει ότι συμβαίνει σε όλο το σώμα του υλικού, ενώ η προσρόφηση παραμένει ένα φαινόμενο επιφάνειας. Η προσρόφηση είναι πάντα εξωθερμική, ενώ η απορρόφηση είναι ενδοθερμική. Η προσρόφηση περιλαμβάνει και τις δύο μεθόδους απορρόφησης και προσρόφησης.
Σύγκριση μεταξύ προσρόφησης και απορρόφησης:
Προσρόφηση | Απορρόφηση | |
Ορισμός | Συσσώρευση αερίου ή υγρού διαλύτη στην επιφάνεια ενός στερεού ή ενός υγρού | Διάχυση μιας ουσίας σε ένα υγρό ή στερεό για να σχηματιστεί ένα διάλυμα ή μια ένωση |
Παράδειγμα | Αδρανή αέρια απορροφούνται σε ξυλάνθρακα. | Ένας ξηρός σπόγγος απορροφά νερό |
Ανταλλαγή θερμότητας | Εξώθερμο με εξαίρεση την προσρόφηση του Η2 σε γυαλί | Ενδοθερμική |
Επίτευξη ισορροπίας | Συγκριτικά γρηγορότερα | Συγκριτικά αργά |
Συγκέντρωση | Η συγκέντρωση στην επιφάνεια του προσροφητικού υλικού είναι διαφορετική από εκείνη του όγκου | Η συγκέντρωση παραμένει η ίδια σε όλο το υλικό |
Ποσοστό εμφάνισης | Είναι ταχεία αρχικά, αλλά αργότερα ο ρυθμός της αρχίζει να μειώνεται | Λαμβάνεται με ενιαίο συντελεστή |